Autores:
Alfredo Jiménez Bernadó y Miguel Angel Simón Marco
Departamentos de Cirugía y Medicina
Facultad de Medicina de Zaragoza
Febrero 2013
La patología biliar representa uno de los capítulos más importantes de la cirugía en general y de la patología abdominal en particular. Las formas de presentación son tan frecuentes como variadas pero hoy día disponemos de recursos clínicos y tecnológicos para llegar a un diagnóstico que nos permita realizar la elección del tratamiento más adecuado.
Anatomía quirúrgica de la vesícula y vías biliares.
La vesícula biliar es un órgano en forma de pera dividido en 3 partes: fondo, cuerpo y cuello, localizándose en esta última parte un pequeño infundíbulo conocido como “bolsa de Hartmann”. Se localiza a nivel de la cara inferior de los segmentos hepáticos IV y V, donde queda cubierta por peritoneo en casi el 70% de su superficie, quedando el resto de la misma apoyada directamente sobre el hígado. Su drenaje se efectúa a través del conducto cístico. El conducto cístico drena directamente a la vía biliar (VB) extrahepática que queda dividida entonces en hepático común, por encima de la desembocadura, y colédoco, por debajo de la misma. La vascularización de la vesícula biliar depende de la arteria cística, rama de la hepática derecha y con la que constituye una interesante relación anatómica, clave a la hora de la colecistectomía, llamada “triángulo de Calot”, que queda constituido por la VB, el cístico y la cística.

Existen variantes anatómicas tanto de la vesícula como de la vía biliar que pueden llegar hasta un 40% de los casos, tanto en su disposición como en sus relaciones con las estructuras anatómicas vecinas. Así por ejemplo la agenesia vesicular (0,03%-0,1% de la población), la presencia de vesículas múltiples (0,025%-0,5%), la desembocadura anómala del conducto cístico, 30%, o las peligrosas anomalías arteriales, 25%, que pueden generar confusiones graves a la hora de la cirugía de esta región.

El colédoco se sitúa a nivel hiliar en el borde derecho externo de la arteria hepática propia, que posteriormente se divide, de modo que la hepática derecha pasa posterior al mismo. Tras un segmento retroduodenal, a la derecha de la arteria gastroduodenal, el colédoco pasa a ser intrapancreático, desembocando, en el 60% de los casos, en la parte media de la segunda porción duodenal. Esta desembocadura puede ser común con la del ducto pancreático o Wirsung en el 60% de los casos, a modo de doble cañón en el 38%, o por separado en un 2%. La desembocadura recibe el nombre de papila duodenal mayor, ampolla de Vater o ampolla hepatopancreática. Esta papila dispone de un pequeño esfínter circular denominado esfínter de Oddi que se encarga de regular el flujo de bilis al duodeno, evita el reflujo del líquido duodenal y envía la bilis a la vesícula. Es una estructura muscular compleja, independiente de la duodenal, que crea una zona de alta presión entre el conducto y el duodeno. Mide 4-6 mm y tiene una presión basal de 5 mmHg mayor que el colédoco, y 15 más que el duodeno. Tiene contracciones fásicas de 12-140 mmHg. Es regulado por las células de Cajal en respuesta a la CCK, y las alteraciones de este mecanismo pueden dar lugar a cólicos biliares.
Fisiología de la vesícula y vías biliares.
La bilis es un líquido compuesto de agua, electrolitos, sales biliares, proteínas, lípidos y pigmentos biliares. Tiene un pH neutro o ligeramente alcalino. El hígado produce 500-1000 ml de bilis al día en respuesta a estímulos neurogénicos, humorales y químicos.
- Estimulación vagal: aumento de la secreción biliar
- Estimulación esplácnica: disminución de la secreción biliar
- HCl, proteínas, ácidos grasos al duodeno: aumentan la secreción de secretina duodenal: aumento de la secreción biliar
El esfínter de Oddi contribuye a almacenar la bilis en la vesícula en periodos de inactividad digestiva. Por el contra, la secreción de CCK provocada por la presencia de ácidos grasos en el duodeno estimula la contracción del músculo liso vesicular y la relajación del esfínter de Oddi, permitiendo el paso de bilis al duodeno. Como la producción de sales biliares es insuficiente necesita reciclarse. Esto lo lleva a cabo mediante la circulación entero-hepática, en la cual se absorben las sales biliares en el íleo hacia la circulación portal. El 95% de la bilis secretada se recicla, y solo se pierde el 5% en las heces, dándoles su color característico.
En ayuno, el 80% de la bilis se almacena en la vesícula. La mucosa vesicular tiene la mayor capacidad absortiva del cuerpo humano. La mucosa segrega lipoproteínas como autoprotección e iones H para bajar el pH de la bilis. Durante la digestión, la vesícula se contrae (CCK) y vacía el 50-70% de su contenido en 30-40 min. Las alteraciones de la actividad motora de la vesícula contribuye a la nucleación del colesterol y la formación de litiasis (también da lugar a dolores cólicos sin necesidad de formación litiásica debido a la alteración motora).
Estudios diagnósticos en patología biliar
Estudios analíticos.-
El diagnóstico principal de la patología biliar se realiza mediante estudios radiológicos, sin embargo se puede sospechar por la alteración que se produces en las “mal llamadas” pruebas de función hepática. La interpretación de los análisis debe de realizarse conjuntamente con la historia clínica y la exploración física. Se incluye: Bilirrubina, F. Alcalina, ALT, AST, GGT, Albúmina gammaglobulina, tiempo de protrombina.
Las pruebas que ponen de manifiesto la patología biliar son las denominadas de colestasis: F alcalina, GGT, bilirrubina y en menor medida las transaminasas.
Fosfatasa alcalina.
Su aumento en la enfermedad hepática es consecuencia de un aumento en la secreción y por eso en los primeros días de una obstrucción biliar puede ser normal. Al ser su vida media de 1 semana una vez resuelta la obstrucción esta permanecerá elevada 1 semana. Se eleva en colestasis y en menor medida en el daño inflamatorio. Los valores más elevados ocurren en las enfermedades colestáticas: cualquier obstrucción de la via biliar intra o extrahepática produce su elevación, pero su valor cuantitativo no permite la diferenciación de la causa que produce la colestasis. En la mayoría de los casos se acompaña de aumento de bilirrubina, los incrementos en escasa cuantía (x2 ó 3) pueden verse en cualquier enfermedad hepática: cirrosis, hepatitis, e incluso insuficiencia cardiaca congestiva.
Gamma Glutamiltranspeptidasa (GGT).
Se localiza en distintos tejidos, riñón, vesiculas seminales, páncreas, bazo, hígado. En hígado están tanto en hepatocitos pero sobre todo en las células epiteliales de los conductos biliares.
Sus valores séricos dependen de la edad y sexo. Son más elevados en hombres que en mujeres y en los adultos aumentan con la edad. Los neonatos pueden tener valores 5-8 veces superiores a los adultos.
Además del daño hepático pueden aumentar en diversos procesos, alcoholismo crónico, enfermedad pancreática, IAM, insuficiencia renal, EPOC y diabetes.
En la enfermedad hepática se correlaciona directamente con los valores de F. Alcalina, de ahí su utilidad para confirmar el origen hepático de la F alcalina. La determinación de GGT es una prueba sesible en detectar daño hepático y la más sensible para detectar enfermedad de conductos biliares.
Es un enzima inducible por drogas, las más conocidas: alcohol, fenitoina.
Bilirrubina.
Su concentración normal es inferior a 1 mg/dl, de predominio no conjugado. Se elimina por orina fundamentalmente la fracción conjugada ya que la No conjugada va unida a la albúmina. En base a esto se clasifica:
El valor sérico de bilirrubina tiene valor pronóstico en la enfermedad hepática y particularmente en la cirrosis biliar primaria, enfermedades colestasticas y en el fallo hepático crónico, en la hepatitis viral aguda tiene una valor pronóstico más limitado.
Métodos radiológicos.-
La radiología simple carece de valor diagnóstico ya que sólo diagnosticaría las litiasis radioopacas y/o algunas de las complicaciones
La ecografía abdominal es la prueba de imagen “patrón oro“ y, generalmente, la única necesaria. Es inocua, de bajo coste y está disponible en la mayoría de los centros. Los cálculos son móviles, declives y con sombra acústica. Su sensibilidad y especificidad son > 95% para los cálculos de vesícula > 4mm y es más baja en la coledocolitiasis.
La colecistografía oral se utiliza, fundamentalmente, cuando la vesícula biliar no se puede identificar mediante ecografía (por ejemplo: cuando está llena de cálculos y contraída) y para valorar la motilidad vesicular y la permeabilidad del cístico antes de iniciar un tratamiento de disolución oral o litotricia.
La Gammagrafía con ácido dimetilimidoacetico con tecnecio 99 puede ser útil en colecistitis

La RMN ofrece una alta sensibilidad y especificidad para el diagnóstico de coledocolitiasis, superior al 90% en la mayoría de las series, aunque la técnica es costosa.
La CPRE no tiene indicación primaria en el diagnóstico de la litiasis biliar, siendo una técnica puramente terapéutica.
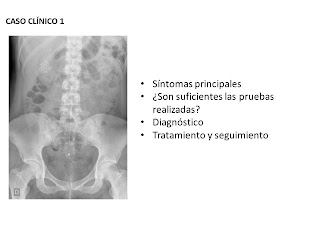
CASO CLINICO 1. Cólico biliar y colecistitis litiásica.
Bases teóricas de la litiasis biliar. Colelitiasis.
La litiasis biliar es una de las principales enfermedades digestivas en la actualidad. Su prevalencia en los países occidentales oscila entre el 10% y el 20%, siendo mayor en edades avanzadas y mujeres. Aunque la mayoría de las litiasis biliares son silentes, en un 20% de los casos aparecen síntomas y/o complicaciones (Tasa anual de 1-4%).
La litiasis biliar es consecuencia de la precipitación de solutos que hay en la bilis: Bilirrubina, sales biliares, fosfolípidos y colesterol. En función de la composición de la litiasis biliar las podemos clasificar en:
- Cálculos de colesterol que representan el 75% de los cálculos en los países occidentales,
- Cálculos de pigmentos marrones (20%) formados fundamentalmente por sales de calcio de bilirrubina no conjugada
- Cálculos de pigmentos negros (5 %) que se asocian típicamente a hemolisis crónica, cirrosis y pancreatitis y cuyo componente principal es el bilirrubinato cálcico.
Los cálculos de colesterol y los de pigmentos negros se forman en la vesícula, mientras que los cálculos de pigmentos marrones se originan en el árbol biliar y la vesícula como resultado de infecciones anaerobias de la bilis o infestaciones parasitarias.
Factores de riesgo de la litiasis biliar.
La prevalencia de colelitiasis tiene una variabilidad geográfica y étnica importante. Es particularmente frecuente en Chile, indios prima y en las poblaciones escandinavas.
Otros factores de riesgo son la edad, el sexo femenino (posiblemente por influencia de los estrógenos) y la obesidad. El uso de fármacos como fibratos, anticonceptivos, octeotrido, la enfermedad de Crohn, enfermedades metabólicas o la cirugía de la obesidad son también factores de riesgo.
Historia Natural
Colelitiasis asintomática
En la mayoría de los pacientes (60-80%), la colelitiasis es asintomática y se diagnostica incidentalmente mediante ecografía realizada por otros motivos. El riesgo medio anual de desarrollar síntomas es del 2-4% y la incidencia anual de complicaciones y cáncer de vesícula es 0,3% y 0,02% respectivamente. Por ello, no es necesario realizar colecistectomía profiláctica.
Colelitiasis sintomática no complicada: Cólico biliar simple.
Una vez presentan cólico biliar el 65% de los pacientes sintomáticos presentaran recurrencia clínica en los 2 primeros años y la incidencia anual de complicaciones es del 1-2%.
Clínica
El cólico biliar se produce por la obstrucción intermitente del conducto cístico por un cálculo y se manifiesta como un episodio de dolor visceral, localizado en epigastrio-hipocondrio derecho, irradiado hacia hombro derecho o escápula, constante, que aumenta gradualmente durante 15 minutos-1 hora, se mantiene durante 1 hora o más y desaparece lentamente. Se puede acompañar de nauseas, vómitos e inquietud. El gas, la distensión abdominal, la flatulencia y la dispepsia no están relacionados con los cálculos en sí mismos. Estos síntomas se encuentran con una frecuencia parecida en pacientes sin colelitiasis y, por tanto, no se debe realizar colecistectomía ante ellos.
Generalmente, la exploración física es normal, aunque puede haber hipersensibilidad en la zona de la vesícula durante el ataque y posteriormente.
Diagnóstico
Los parámetros de laboratorio son normales.
La ecografía abdominal es la prueba de imagen “patrón oro“ y, generalmente, la única necesaria. Es inocua, de bajo coste y está disponible en la mayoría de los centros. Los cálculos son móviles, declives y con sombra acústica. Su sensibilidad y especificidad son > 95% para los cálculos > 4mm.
Complicaciones
Las complicaciones de la colelitiasis incluyen: colecistitis aguda, coledocolitiasis que puede producir colangitis o pancreatitis aguda biliar, fístulas biliares, síndrome de Mirizzi, vesícula en porcelana e incluso la neoplasia vesicular.
Tratamiento
Durante el episodio de cólico biliar se aconseja reposo digestivo, calor local y analgesia. Se recomienda el uso de metamizol y/o AINES, ya que además de aliviar los síntomas, parecen prevenir la progresión del cuadro hacia una colecistitis aguda.
Tras la presentación de un primer episodio de cólico biliar se debe proponer la realización de colecistectomía diferida. En cuanto a la técnica quirúrgica, se recomienda la colecistectomía laparoscópica ya que permite una menor estancia hospitalaria sin que existan diferencias significativas en cuanto a la tasa de complicaciones y/o mortalidad.
El tratamiento no quirúrgico presenta baja eficacia y altas tasas de recurrencia. Por ello, sólo debería ofrecerse a aquellos pacientes con alto riesgo quirúrgico o que no deseen someterse a cirugía. El tratamiento médico más usado actualmente es el tratamiento oral disolutivo. Se utiliza ácido ursodesoxicólico (a dosis de 8-10 mg/Kg de peso/día, antes de acostarse). Este ácido disuelve los cálculos, disminuyendo la secreción biliar de colesterol y desaturando la bilis. Este tratamiento únicamente es aplicable a pacientes muy seleccionados (< 15% de los pacientes sintomáticos). Tiene una eficacia del 20-70% de los pacientes con una recidiva del 50% a los 5 años.
La colelitiasis asintomática no requiere tratamiento quirúrgico, si bien existen excepciones a esta recomendación:
• Pacientes con alto riesgo de desarrollar cáncer de vesícula:
- Existencia de pólipos vesiculares con crecimiento rápido o > 1 cm.
- Cálculo mayor de 3 cm
- Vesícula en porcelana
• Pacientes con riesgo mayor de desarrollar síntomas:
- Joven con anemia drepanocítica. En estos pacientes las crisis de dolor abdominal podrían hacer difícil el diagnóstico diferencial con un cólico biliar o colecistitis aguda.
• Incidental durante la cirugía.
Colecistitis aguda.-
La colecistitis aguda es una entidad clínica caracterizada por la inflamación de la pared vesicular. Su mortalidad global está en torno al 10%, siendo mayor en las formas acalculosas, en pacientes ≥ 75 años y en presencia de ciertas comorbilidades (diabetes, inmunodeprimidos…)
Etiopatogenia
La litiasis biliar es la causante del cuadro en el 90% de los pacientes. Dos factores determinan la progresión a colecistitis aguda: el grado y duración de la obstrucción. Si la obstrucción es completa y duradera se producirá un aumento en la presión intravesicular asociado a la irritación mucosa, activación de la respuesta inflamatoria aguda y disminución del flujo vascular de la pared secundario a la distensión. La infección de la bilis probablemente tiene un papel aditivo, pero secundario, ya que sólo el 20-50 % de los pacientes la presentan. Los microorganismos hallados más comúnmente son: Escherichia coli, Klebsiella pneumoniae, Enterococcus faecalis , Enterobacter spp y Streptococcus faecalis. En los casos más graves pueden encontrarse también anaerobios como Bacteroides fragilis o Clostridium perfringens… 8
Clínica
El síntoma principal es el dolor abdominal agudo, constante, en HCD, de duración mayor de 5 horas, irradiado a espalda, y que se acompaña frecuentemente de náuseas, vómitos y fiebre que oscila entre 37,5ºC y 39ºC. En la exploración física destaca un área de hipersensibilidad en HCD y la palpación manual durante la inspiración profunda a ese nivel produce dolor y cese inspiratorio (signo de Murphy). En pacientes ancianos, especialmente si son diabéticos, el cuadro clínico puede no ser tan típico e incluso no presentar dolor abdominal por lo que es preciso un elevado índice de sospecha.
Algunos signos, como inestabilidad hemodinámica, fiebre alta, acidosis metabólica o íleo indican mayor gravedad y debería descartarse la presencia de colecistitis gangrenosa y/o perforación vesicular
Diagnóstico
Pruebas de laboratorio
Analíticamente se caracteriza por leucocitosis con neutrofilia e incremento de la proteína C reactiva (PCR). Se puede producir también, un incremento leve de transaminasas y amilasa, normalmente inferiores a 3 veces la normalidad, y hasta en un 20% de casos, sobretodo en pacientes con CA grave, ictericia con niveles de bilirrubina inferiores a 4 mg/ dl.
Pruebas de imagen
La técnica de elección es la ecografía abdominal y es suficiente para confirmar el diagnóstico en la mayoría de los casos. Su sensibilidad y especificidad son del 88% y 80% respectivamente, y a pesar de que es una técnica operador dependiente, tiene un valor predictivo positivo del 92%.
La gammagrafía con derivados del ácido iminodiacético ( HIDA) marcado con Tc puede ser de utilidad cuando existe duda diagnóstica a pesar de la exploración ecográfica. La TC abdominal sólo es necesaria si se sospechan complicaciones.
TRATAMIENTO
El manejo de la CA precisa de ingreso hospitalario, reposo en cama, dieta absoluta, fluidoterapia, antibioterapia y analgesia.
o ANALGESIA. Se recomienda el uso de AINES que además de aliviar el dolor, podrían alterar la historia natural del cuadro.
o ANTIBIOTERAPIA (ATB). El tratamiento con ATB es aconsejable salvo en los casos leves que se podría optar por la observación y el tratamiento con AINES. Si se reciben cultivos positivos para algún germen no cubierto se debe modificar la pauta. En los casos leves- moderados podría ser suficiente con una monoterapia con piperacilina/ tazobactam ( 4/0,5 gr iv/ 8horas ) En los casos más graves se deben administrar ATB de mayor espectro. De primera elección serían las cefalosporinas de tercera/cuarta generación asociadas a metronidazol.
Tratamiento quirúrgico.
La colecistectomía es el tratamiento de elección para la CA, ya que si bien casi el 50% de los casos se podrían resolver mediante tratamiento médico, un 20% de los pacientes reingresarían por eventos similares.
En los pacientes de alto riesgo quirúrgico con enfermedades graves, como insuficiencia hepática, pulmonar o cardíaca, es preferible la colecistostomía que la colecistectomía. Tras resolverse el cuadro se debería realizar colecistectomía laparoscópica si el estado general del paciente lo permite.
El “cómo” y el “cuándo” realizar la colecistectomía ha sido tema de debate durante años. La colecistectomía por vía abierta de forma temprana (en los primeros 5 días desde la aparición de los síntomas) no incrementa la morbi-mortalidad respecto a la cirugía diferida (a partir de la 6ª semana) y presentaba una menor estancia hospitalaria y un menor tiempo de intervención quirúrgica. Sin embargo, la cirugía diferida incrementaba el riesgo de nuevas complicaciones de origen biliar en el tiempo de espera.
Colecistitis aguda litiásica
Alrededor del 10 % de las CA ocurren en ausencia de cálculos biliares. En la mayoría de las ocasiones sucede en pacientes en estado crítico, o bien asociada a diabetes mellitus, insuficiencia cardíaca congestiva, insuficiencia renal terminal o SIDA.
La tasa de mortalidad está en torno al 30 %, debido en parte a su rápida evolución a gangrena y perforación.
Aunque la colecistectomía ha sido históricamente el tratamiento de elección, actualmente la colecistostomía percutánea se ha convertido en una alternativa eficaz y mínimamente invasiva, sobre todo en pacientes de alto riesgo quirúrgico. En caso de no obtenerse una mejoría a las 3 semanas de la colocación del drenaje, se debería reconsiderar el diagnóstico, y en caso de confirmarse, se debería realizar una colecistectomía de forma urgente.
Colecistitis enfisematosa
Es una entidad poco frecuente, con una mortalidad en torno al 15%. Es más prevalente en el sexo masculino y en pacientes con diabetes mellitus y enfermedad vascular periférica. La ecografía posee una sensibilidad y una especificidad menores que la radiografía simple o que la TC. Los gérmenes aislados con mayor frecuencia son Clostridium y E. Coli. La colecistectomía inmediata es el tratamiento de elección.
CASO CLINICO 2. Coledocolitiasis post colecistectomía.
Bases teóricas de la coledocolitiasis y sus complicaciones.
La coedocolitiasis se define como la presencia de cálculos en los conductos biliares. Los cálculos de la vía biliar pueden provenir de la vesícula biliar o formarse en el conducto. En los países occidentales, el 95 % de los pacientes con coledocolitiasis tienen también colelitiasis. A la inversa, el 15 % de los pacientes con colelitiasis tienen coledocolitiasis.
Clínica
Sólo el 10% de los pacientes con coledocolitiasis permanecen asintomáticos durante años, pero las pruebas disponibles indican que su evolución natural no es tan benigna como en las colelitiasis asintomáticas.
La obstrucción biliar por cálculos suele ser incompleta. Cuando se produce de forma aguda, el paciente presenta dolor, similar al del cólico biliar simple, aunque generalmente más prolongado, e ictericia, habitualmente moderada y de curso intermitente. Si la obstrucción se desarrolla gradualmente se puede manifestar como prurito o ictericia solamente. En las obstrucciones de larga duración (> 5 años) puede producirse cirrosis biliar secundaria.
Diagnóstico
Pruebas de laboratorio
Se suele objetivar incremento de GGT y FA (en 94% y 91% respectivamente) e hiperbilirrubinemia, a expensas de bilirrubina directa. El incremento de bilirrubina es proporcional al grado de obstrucción. Generalmente, está en torno a 2 y 5 mg/ dl y no suele superar los 12 mg/dl.
Pruebas de imagen
La obstrucción de la vía biliar produce dilatación que se puede detectar mediante pruebas de imagen.
Ecografía abdominal
Es la exploración inicial de elección, pero solo se visualizan las coledocolitiatis en un 50 % de los casos. Sin embargo, la sensibilidad para detectar la dilatación del colédoco (> 6 mm en pacientes con vesícula y > 8 mm en colecistectomizados) es de un 75% aproximadamente 2.
Ecoendoscopia y Colangio-resonancia
Tienen una sensibilidad y especificidad para detectar CDL comparables con la colangiopancreatografía retrograda endoscópica (CPRE). Su principal inconveniente es que son pruebas sin posibilidad terapéutica.
CPRE
Es considerada la prueba patrón oro para el diagnóstico y tratamiento de la CDL y tiene una sensibilidad y especificidad del 95% aproximadamente. Sin embargo, cuando la probabilidad de CDL es baja, deber realizarse primero otros estudios menos invasivos. Imagen 5
Tratamiento
La coledocolitiasis se asocia a una elevada tasa de complicaciones graves, incluso en pacientes asintomáticos por lo que se recomienda realizar tratamiento en casi todos los casos.
Existen varias opciones de tratamiento que incluyen el tratamiento de disolución, las técnicas de intervención radiológicas y endoscópicas y la cirugía. La estrategia más adecuada dependerá de muchos factores: presentación clínica, comorbilidad del paciente, experiencia de los especialistas, técnicas disponibles... (Figura 3).
CPRE terapéutica
Generalmente es el tratamiento de elección. La esfinterotomía es el tratamiento que más se usa en la CLD y tiene éxito en más del 90% de los casos. Consiste en la sección del esfínter biliar de la papila y el infundíbulo papilar. Una vez abierto, los cálculos pueden salir de forma espontánea, o bien se extraen mediante cestas de alambre o un balón de oclusión. La CPRE terapéutica presenta una tasa de mortalidad inferior al 1% y una tasa de complicaciones del 5-10%: hemorragia digestiva, pancreatitis, colangitis y perforación retroduodenal. Su aplicación está limitada en pacientes con divertículos duodenales, en pacientes con coledocoyeyunostomía en Y de Roux, en gastrectomizados con reconstrucción tipo Billroth II y cuando existen cálculos de gran tamaño (> 2cm).
Colangitis aguda
Es una infección sistémica grave que tiene como origen la infección del árbol biliar. Para que se produzca es necesaria la obstrucción y la infección biliar.
La coledocolitiasis es la causa más frecuente de colangitis (85%), pero hay otras otras causas de obstrucción (estenosis biliares benignas o malignas, infecciones parasitarias, anomalías congénitas de los conductos biliares…) que pueden producirla. Cuando la obstrucción es completa, como suele ocurrir en las estenosis malignas, es más difícil que se produzca reflujo duodeno-biliar de bacterias, siendo menos frecuente la aparición de CLA en estos casos.
Generalmente, las bacterias aisladas en bilis tienen un origen gastrointestinal. Las bacterias aeróbicas aisladas más frecuentemente son Echerichia coli, Klebsiella, Enterococcus y Enterobacter.
CLÍNICA
Clínicamente se caracteriza por dolor abdominal en hipocondrio derecho o epigastrio, fiebre, generalmente alta y con escalofríos, e ictericia (Triada de Charcot). Cuando se añade confusión metal y shock se denomina Pentada de Reynolds, generalmente asociada a una colangitis grave y alta mortalidad. La fiebre y el dolor abdominal son los signos más frecuentes, presentando una incidencia cada uno de ellos del 80% o más. Sin embargo, la ictericia solo se observa en un 60-70 % de los casos. La incidencia de la triada completa es menor al 70% y la Pentada de Reynolds es extremadamente rara (3,5 %-7,7% de los pacientes).
El diagnóstico de CLA se basa en la asociación de signos y síntomas de infección con los propios de una obstrucción biliar.
TRATAMIENTO
El tratamiento de la colangitis aguda se dirige hacia los dos componentes etiológicos del cuadro: la obstrucción y la infección. Así, se basa en la combinación de antibioterapia y el drenaje biliar.
Tratamiento antibiótico
En todos los pacientes en los que se sospeche una colangitis aguda se debe comenzar tratamiento antibiótico empírico tan pronto como sea posible y tras extraer hemocultivos.
La pauta más aceptada en el momento actual es la combinación de una penicilina de amplio espectro con un inhibidor de beta-lactamasa, como por ejemplo: piperacilina-tazobactam 4,5 gramos/ 6 horas.
En aproximadamente un 80% de los casos, la infección se controla mediante tratamiento médico (el estado del paciente mejora en 6-12 horas), permitiendo una evaluación etiológica y un manejo electivo similar a los casos de ictericia sin colangitis. Sin embargo, en un 15% de los casos el estado clínico empeora y es obligado realizar un drenaje biliar precoz.
Drenaje biliar
Métodos de drenaje
El drenaje biliar se puede realizar mediante CPRE o cirugía abierta. Mediante CPRE se pueden colocar prótesis o drenajes nasobiliares que serían suficientes para lograr un adecuado drenaje biliar. La adicción de esfinterotomía es recomendable, si las condiciones del paciente lo permiten, ya que en muchas ocasiones será el tratamiento definitivo.
¿Cuándo realizar el drenaje?
Si la colangitis aguda es grave o moderada debería realizarse lo antes posible. Para los casos leves, que responden favorablemente al tratamiento médico, se recomienda realizarlo en las primeras 24-48 horas.
CASO CLINICO 3. Colangiocarcinoma hiliar tipo I.
Bases teóricas de los cánceres de vesícula y vías biliares.
Después de la litiasis los tumores son los procesos quirúrgicos más frecuentes de las vías biliares. Son poco frecuentes en nuestro medio pero su incidencia está aumentando probablemente por el mayor uso y la precisión de las nuevas tecnologías de la imagen.
El tipo histológico más frecuentes es el adenocarcinoma (90%) seguido del cistoadenocarcioma y aunque también existen tumores benignos no haremos mención a ellos por ser una auténtica rareza.
Se presentan generalmente con una sintomatología inespecífica hasta estadios avanzados en que la ictericia y el síndrome tóxico son evidentes.
Topográficamente se clasifican en:
- Tumores de la vesícula biliar que suponen entre el 75% y 80% de todos ellos
- Tumores de la vía biliar principal (10%) en los que habrá que distinguir entre los del tercio superior (confluente de los hepáticos conocido habitualmente como tumor de Klatskin), los del tercio medio que afectan al colédoco desde el cístico hasta la entrada en el páncreas y los del tercio inferior o colédoco intrapancreático
- Tumores ampulares, periampulares o también llamados de la encrucijada biliopancreática (10%), que son díficiles de clasificar con precisión y de diferenciar su origen en la ampolla, en la vía biliar, en el páncreas o en el duodeno. Aunque en ocasiones se estudian asociados al carcinoma pancreático, haremos mención a ellos tras el desarrollo del caso clínico nº 4.
CANCER DE VESÍCULA BILIAR.
Tiene una incidencia variable desde 1,2 casos/100.000 hab/año en EE.UU. a 7,5 casos en Chile. Predomina en la mujer sobre el varón en la proporción 4:1. Es el cáncer biliar más común como ya hemos dicho pero tiene muy mal pronóstico (su supervivencia global no llega al 10% a los 5 años), debido a su facilidad para diseminarse desde la mucosa de la vesícula invadiendo el lecho vesicular hepático y luego el hilio hepático y a su vez la rápida diseminación linfática, hematógena y peritoneal, formando un voluminoso bloque tumoral inoperable.

La asociación del carcinoma de vesícula biliar con la litiasis biliar en un hecho conocido y sucede entre el 70 y 90% de los casos, por lo que cabría pensar en el papel que la litiasis pueda jugar en la génesis del tumor. Aunque no existe ningún trabajo experimental que haya demostrado esta relación, parece que la litiasis de larga duración puede suponer un estado precursor del cáncer vesicular por lo que deberemos considerar que el riesgo de cáncer aumenta con la duración de la enfermedad calculosa y con la edad del paciente. En cambio, no tiene nada que ver, ni supone mayor riesgo, el hecho de que la litiasis sea sintomática o asintomática.
El carcinoma de vesícula tiene tres formas clínicas de presentación:
- Hallazgo inesperado en el transcurso de una colecistectomía rutinaria en una paciente con una historia biliar más o menos antigua. Incluso en ocasiones es el patólogo el que lo descubre con el estudio de la pieza.
- Debuta con una ictericia progresiva como consecuencia de que el crecimiento tumoral afecta a la vía biliar principal.
- En ausencia de ictericia, la exploración clínica muestra un plastrón vesicular duro y grande e incluso una carcinomatosis peritoneal.
El diagnóstico en estadios precoces es difícil porque tanto la ecografía como la TAC son poco sensibles e inespecíficos. Cuando existe clínica la primera exploración suele ser la ecografía que aunque raramente ve el tumor ofrece datos de sospecha diagnóstica como es la existencia de dilatación de las vías biliares intrahepáticas, el estado de la vesícula con o sin litiasis. La TAC helicoidal multicorte suele ser suficiente para llegar al diagnóstico y realizar una estadificación preoperatoria que permita conocer las posibilidades de tratamiento del caso.
La estadificación TNM del carcinoma de vesícula biliar según la Unión Internacional Contra el Cáncer (UICC) se expone en la Tabla siguiente:
En otras asociaciones como la AJCC los tumores T3 son los que invaden directamente el hígado y/o órganos adyacentes y los T4 son los que invaden la vena porta o la arteria hepática.

La mayoría de los tumores de la vesícula biliar se diagnostican en estado avanzado y las posibilidades terapéuticas son muy bajas. Cuando se descubre en el curso de una colecistectomía por litiasis biliar, la extirpación de la vesícula puede ser suficiente para los tumores pTis o pT1. En cambio en los tumores pT2, dada la ineficacia de la radioterapia y de la quimioterapia, es recomendable recurrir a una cirugía de rescate llevando a cabo una segmentectomía hepática que incluya el segmentos IVb y V junto con una amplia linfadenectomía, aunque existen controversias dada la morbimortalidad de este tipo de cirugía. En tumores avanzados las posibilidades quirúrgicas se reducen de manera considerable requiriendo, si es técnicamente posible, amplias hepatectomías con exéresis de la vía biliar y linfadenectomías extensas, intervenciones todas ellas con elevada complejidad, morbimortalidad desproporcionada con la habitual edad avanzada de estos pacientes y el mal pronóstico general de este tumor. En aquellos casos en que exista ictericia, si la exéresis no es posible puede intentarse algún tipo de derivación biliodigestiva o en su defecto una intubación transtumoral por Radiología Intervencionista, para aliviar la sintomatología.
CANCER DE LA VÍA BILIAR EXTRAHEPÁTICA.
La incidencia de este tipo de tumor está entre 1 caso por 100.000 habitantes/año en EE.UU., 5,5 en Japón y 7 casos en Israel. Se iguala bastante la relación mujer/hombre, 1.2:1 y su predominio es el entorno de la bifurcación de los hepáticos (placa hiliar), más del 60% de los casos (esta especial localización se conoce como tumor de Klatskin). Tan solo un 25% de los casos afectan al tercio medio o distal de la vía biliar.
Es también un tumor de mal pronóstico aunque en los últimos tiempos se tiende hacia un tratamiento quirúrgico más agresivo, debido a que su crecimiento es muy lento y a menudo causan la muerte más por obstrucción biliar y fallo hepático que por la progresión del cáncer. No obstante un tercio de los pacientes ya tienen metástasis en el momento del diagnóstico pero su progresión lenta habitual permite tratamientos paliativos de larga duración. En su lento crecimiento se extiende preferentemente por los ductos biliares, pero también acaba afectando al hígado, estructuras vasculares hiliares, metástasis peritoneales e intrahepáticas.

La forma clínica más habitual en las lesiones hiliares se caracteriza por una ictericia progresiva indolora (90%), con prurito, pérdida de peso (29%), dolor abdominal vago (20%), fatiga o náuseas. Puede presentarse en algunos casos una colangitis con sepsis resultante de la contaminación bacteriana de la bilis obstruida. En los casos que afectan al tercio medio o distal se encuentra una vesícula distendida (signo de Courvoisier-Terrier), palpable en el examen abdominal a diferencia de los que ocurre en los tumores hiliares.

Tanto la ecografía, como la CPRE y la TAC son medios diagnósticos muy sensibles a la hora de detectar la dilatación biliar y además la última es capaz de darnos información acerca la extensión de la enfermedad local, regional y a distancia, e incluso la posible afectación de las estructuras vasculares (vena porta, arteria hepática) que va a condicionar la resecabilidad. Sin embargo ninguno de ellos suele ver de manera clara el tumor salvo en estadios avanzados. En la mayoría de los casos los pacientes van al quirófano con un diagnóstico de presunción sin confirmación por anatomopatológica, dado que tan solo se puede obtener tejido mediante el cepillado de la vía biliar durante la CPRE y muy excepcionalmente por punción dirigida. En más del 50% de los casos no se tiene confirmación patológica antes de la cirugía.

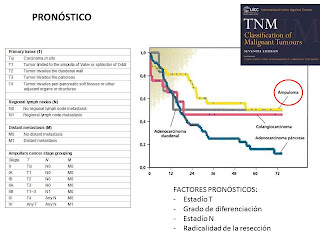
El estadiaje de este tipo de tumor suele hacer según la clasificación de la AJCC según los criterios TNM de cara al pronóstico de estos tumores. Sin embargo desde el punto de vista del tratamiento quirúrgico la clasificación de Bismuth-Corlette en la que nos orienta sobre las diversas opciones quirúrgicas en la forma más frecuente, el tumor de Klatskin:

El cáncer de la vía biliar extrahepática es de difícil tratamiento. La resección quirúrgica cuando es posible ofrece la única posibilidad de supervivencia a largo plazo y es posible hacerlo enre el 10 y 85% de los casos dependiendo si se tienen en cuenta o no los cánceres distales. Los tumores del tercio distal tienen los mejores criterios de resecabilidad por medio de la duodenopancreatectomía cefálica (operación de Whipple). Los tumores del tercio medio son poco frecuentes y precisarían una resección completa de la vía biliar, vesícula y una hepaticoyeyunostomía para la reconstrucción del tránsito biliar, todo ello asociado a una linfadenectomía. En los tumores de Klatskin, el tipo I se beneficiaría de una resección completa de la vía biliar y vesícula con hepaticoyeyunostomía en la placa hiliar o según otras experiencias debería ser asociarse al igual que en los tipos II y IIIa a una hepatectomía derecha ampliada al segmento IV. Por el contra en el tipo IIIb debería asociarse una hepatectomía izquierda ampliada al segmento V. Se debe de incluir siempre la resección del segmento I porque los conductos biliares de dicho segmento drenan directamente en la confluencia y son los primeros en quedar englobados por el tumor.

Por lo general las lesiones tipo IV se considerar irresecables y solo podrían beneficiarse de algún tipo de derivación biliodigestiva o en su defecto de una intubación transtumoral con prótesis rígidas o autoexplandibles para salvar la estenosis biliar.
Algunos estudios con el trasplante hepático en el colangiocarcinoma con resultados poco alentadores por la una alta tasa de recidiva a medio plazo y supervivencia desalentadora a los 5 años, 23%. No obstante la Clínica Mayo ha publicado supervivencias más altas con un protocolo muy estricto de estadificación preoperatoria y quimioradioterapia neoadyuvante, resultados pendientes de ser reproducidos en otros centros.
CASO CLINICO 4. Tumor ampular.
Bases teóricas de los cánceres del área ampular.
Los tumores de la ampolla de Vater se denominan ampulomas, representan el 2% de todos los tumores del tracto digestivo y se pueden originar sobre cualquiera de los tres epitelios (duodenal, pancreático y biliar) que conforman la papila. Estos tumores tienen una especial relevancia clínica, por lo que es fundamental realizar un diagnóstico precoz, una estadificación apropiada y un tratamiento correcto. Los ampulomas presentan un mejor pronóstico y una mayor tasa de resecabilidad, en comparación con otros tumores peripapilares, gracias a que presentan síntomas de forma más precoz y a que tienden a ser más diferenciados desde el punto de vista histológico.

Los tumores de la papila de Vater se pueden clasificar en benignos: adenomas tubular, tubulovelloso y velloso, lipoma, fibroma, linfangioma, leiomioma y hamartoma y malignos: adenocarcinoma, linfoma y tumor neuroendocrino o carcinoide. En la papila también pueden metastatizar otros tumores: melanoma maligno, hipernefroma y linfoma. El tumor más frecuente es el adenoma, y su progresión a adenocarcinoma esta´ admitida en el mismo sentido que la secuencia adenoma-carcinoma de los pólipos de colon. El método habitual de estudio histológico con pinza de biopsia ha demostrado sus limitaciones para descartar la presencia de focos de adenocarcinoma, dado que no es infrecuente la coexistencia de adenoma y adenocarcinoma en el mismo tumor papilar.

FORMAS CLÍNICAS. Puede ser totalmente inespecífica. Cuando está presente, responde a la obstrucción biliar o pancreática. El síntoma clínico más frecuente es la ictericia (en un 50% de los casos), seguida por dolor abdominal más o menos intenso (en una 30%). En ocasiones puede asociarse pancreatitis aguda, anemia ferropénica, hemorragia digestiva y colangitis. La ictericia intermitente, secundaria a necrosis tumoral, asociada a hemorragia digestiva es la manifestación clínica que más orienta hacia el diagnóstico de ampuloma. Los pacientes con tumores malignos pueden asociar un síndrome constitucional con astenia, anorexia y pérdida de peso.
Los datos de laboratorio aportarán un patrón de colestasis más o menos acentuada y variable, con ascenso de la bilirrubina total y directa, fosfatasa alcalina y transaminas. En aquellos casos en los que se asocie sangrado de la lesión es posible encontrar una anemia ferropénica.
El diagnóstico por la imagen suele iniciarse por una ecografía abdominal que por lo general tan solo demuestra dilatación de la vía biliar intra y extrahepática, asociada o no a colelitiasis. En la mayoría de los casos es la C.P.R.E. la prueba de imagen fundamental que va a permitir afinar el diagnóstico. Permite ver directamente la tumoración, realizar el estudio radiológico para ver el estado de la vía biliar, tomar una biopsia o incluso la exéresis completa en lesiones de pequeño tamaño y sin aspecto infiltrativo.

La colangioresonancia no aporta más datos de interés que la ecografía y la CPRE juntas. La realización de una TAC helicoidal será de interés como valoración preoperatoria y estudio de extensión. En cuanto a la ecoendoscopia, no aporta datos añadidos en tumores de < 1 cm, pero por encima de este tamaño es la prueba más sensible para el estadiaje tumoral con una sensibilidad del 75% en la determinación de la T, aunque baja para la determinación de la afectación ganglionar y ductal.
El estadio tumoral, el grado de diferenciación y la presencia de invasión linfática son los principales factores pronóstico del tratamiento quirúrgico. El pronóstico de los ampulomas malignos es superior al de los adenocarcinomas pancreáticos, con una supervivencia a los 5 años del 35–67%.

Las opciones quirúrgicas de elección para los tumores malignos de la ampolla de Vater son dos: la duodenopancreatectomía cefálica y la ampulectomía quirúrgica, ésta última reservada tan solo para tumores de menos de 2 cm y pacientes añosos con factores de riesgo quirúrgico importantes. La ampulectomía endoscópica es una técnica que tiene que limitarse a centros de referencia con endoscopistas expertos. Es una opción que sólo es posible cuando el tumor se limita a la mucosa y/o la submucosa (T0 o Tis, y T1 sin invasión linfática). La paliación terapéutica en tumores irresecables se basa en la práctica de una CPRE para tomar biopsias, con esfinterotomía y ampulectomía endoscópica en tumores muy vegetantes, seguidas de la inserción de una prótesis que se recomienda sea de malla autoexpandible dada la larga supervivencia de estos pacientes.
BIBLIOGRAFIA:
-J.A. Fernández Hernández, P. Parrilla Paricio. El paciente con patología de las vías biliares. En: Cirugía biliopancreática. Guías clínicas de la Asociación Española de Cirujanos. Adan Ediciones. Madrid 2009. pgs 21-37.
-D. Casanova Rituerto. Cirugía de la litiasis biliar. En: Cirugía biliopancreática. Guías clínicas de la Asociación Española de Cirujanos. Adan Ediciones. Madrid 2009. pgs 39-61.
-J. Figueras Felip. Cáncer de vesícula y vías biliares. En: Cirugía biliopancreática. Guías clínicas de la Asociación Española de Cirujanos. Adan Ediciones. Madrid 2009. pgs 99-113.
-V. Lorenzo-Zuñiga, V. Moreno de Vega, E. Domenech y J. Boix. Diagnóstico y tratamiento de los tumores de la papila de Vater. Gastroenterol Hepatol 2009; 32(2):101-108.
-B. Blechacz, M. Komuta, T. Roskans and G.J. Gores. Clinical diagnosis and staging of cholangiocarcinoma. Nat Rev Gastroenterol Hepatol 2011; 8(9):512-522.
-R. Castaño Llano. Tumor de la confluencia hiliar hepática (Klatskin). Rev Col Gastroenterol 2011; 26(2):121-130.